Опыт применения терапии билатерального гонартроза препаратом АМБЕНЕ® БИО
Лечение остеоартрита представляет собой серьезную проблему ввиду высоких показателей заболеваемости, инвалидизации, частого сочетания с соматической патологией, возможными побочными эффектами и осложнениями противовоспалительной терапии. Многие научные исследования направлены на поиски альтернативных путей решения данной проблемы. В статье рассмотрен случай лечения билатерального остеоартрита коленных суставов препаратом АМБЕНЕ® БИО
Остеоартрит (ОА) — гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц [1]. Это хроническое прогрессирующее заболевание, течение которого на протяжении нескольких или десятков лет приводит к инвалидности — больные с деформирующим артрозом составляют около одной трети всех лиц со стойкой утратой трудоспособности в результате заболеваний суставов [2].
Гонартроз (ГА) — артроз коленного сустава, причина развития которого заключается в несоответствии между механической осевой нагрузкой на нижнюю конечность и способностью структурных элементов коленного сустава противостоять этой нагрузке [3].
Частота ГА среди взрослого населения мира варьирует при учете лишь клинических критериев от 2,0 до 42,4% и рентгенологических — от 16,3 до 33,0% [4, 5]. По данным официальной статистики, в России гонартрозом и (или) коксартрозом страдает 13% населения [4], а с 2000 по 2010 год в Российской Федерации число больных ОА увеличилось почти в 2,5 раза [5].
Остеоартрит — основная причина длительной нетрудоспособности у людей старше 65 лет [3]. В этой возрастной группе накапливаются и коморбидные заболевания: артериальная гипертония, ишемическая болезнь сердца, ожирение, сахарный диабет, которые, с одной стороны, поддерживают течение ОА, с другой — затрудняют проведение адекватного обезболивания при ОА.
Установлено, что в основе патогенеза остеоартрита лежат нарушение нормального обмена хрящевой ткани в виде преобладания процессов катаболизма хряща на фоне замедленной его репарации и увеличение синтеза провоспалительных цитокинов. Теория воспаления, ассоциированного с возрастом (low-grade inflammation), — одна из ведущих в изучении прогрессирования остеоартрита [6].
Воспалительный компонент приводит к нарушению фильтрации через мембрану гиалуроновой кислоты, ее вымыванию из полости сустава и прогрессированию дегенерации хряща. Провоспалительные цитокины вызывают деградацию матриксных макромолекул, ингибируют синтез протеогликанов и коллагена. Таким образом, к механизмам развития ОА относятся не только механическое поражение сустава и дегенеративный процесс, но и сопутствующее хроническое воспаление (хоть и не такое острое, как при артрите), способствующее разрушению гиалинового хряща [7]. При этом в патологический процесс вовлекаются как все компоненты сустава [8], так и структуры центральной нервной системы, связанные с формированием хронического болевого синдрома. Секреция провоспалительных цитокинов приводит и к прогрессированию остеоартрита, и к развитию сердечно-сосудистой патологии (в частности, атеросклероза), и когнитивным нарушениям [9].
В последние годы подтверждено: ОА ассоциируется с увеличением риска смерти [10], что объясняется, помимо низкоинтенсивного хронического воспаления, лежащим в основе патогенеза ОА, длительным болевым синдромом и высокой коморбидностью [11].
В настоящее время выделены определенные фенотипы остеоартрита, и это позволяет использовать персонифицированный подход к терапии [12], учитывающий распространенность ОА, а также коморбидность: сердечно-cосудистую и желудочно-кишечную патологию, немощность, депрессивные расстройства, генерализованную боль. Важное значение в патогенезе ОА отводится ожирению. Снижение веса при наличии избыточной массы тела (ИМТ ≥25 кг/м2) на 10–12% не только способствует уменьшению механической нагрузки на коленный сустав. Жировая ткань, будучи самостоятельным секреторным органом, выделяет множество биологически активных веществ — провоспалительных адипокинов (лептин, резистин, висфатин). Одновременно снижаются уровни противовоспалительных адипокинов, тем самым поддерживая низкоинтенсивное хроническое воспаление, которое является патогенетическим звеном ОА и сердечно-сосудистой патологии [3]. Таким образом, ведущими направлениями патогенетического лечения ОА являются:
- модуляция воспаления;
- стимуляция синтеза хряща;
- уменьшение болевого синдрома.
Это еще один не менее важный аспект терапии, поскольку подавляющее число больных ОА страдают от хронических болей. Новые представления о патогенезе остеоартрита позволяют разрабатывать современные таргетные препараты с действием, направленным на воспалительный процесс, связанный со старением. Это, в свою очередь, помогает предотвратить развитие или облегчить течение ряда возраст-ассоциированных заболеваний. Диагностика остеоартрита базируется на выявлении клинических признаков поражения сустава. Диагноз устанавливается на основании жалоб и анамнестических данных больного, клинико-инструментального исследования. С помощью инструментальных методов можно определить степень прогрессирования и деструкции.
За последнее десятилетие рекомендации по лечению ОА опубликовали различные международные и национальные сообщества: Европейский альянс ассоциаций ревматологов (EULAR, 2013, 2018); Международное общество по изучению остеоартрита (Osteoarthritis Research Society International, OARSI, 2010, 2014, 2019); Европейское общество по клиническим и экономическим аспектам остеопороза, остеоартрита и мышечно-скелетных заболеваний (European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases, ESCEO, 2014, 2016, 2019); Ассоциация ревматологов России (АРР, 2017, 2021); Российское научное медицинское общество терапевтов (РНМОТ, 2016) и др. Несмотря на широкую представленность рекомендаций, ведение пациентов с ОА до сих пор остается сложным вопросом. Международные и национальные клинические рекомендации по лечению ОА определяют последовательность действий врача с использованием доказательной базы для различных препаратов [3, 13, 14]. Пациентам с ОА рекомендована немедикаментозная терапия на всем протяжении ведения больного. Она включает, помимо образовательных программ, лечебной физкультуры и снижения массы тела, коррекцию нарушенной оси сустава (варусной/вальгусной) с помощью ортопедических приспособлений (ортезы, супинаторы), разгрузку суставов при поздних стадиях ОА (использование трости, костылей, ходунков и т. п.).
В настоящее время выделены определенные фенотипы остеоартрита, и это позволяет использовать персонифицированный подход к терапии
В качестве базисной медикаментозной терапии рекомендованы две основные группы лекарственных препаратов: симптом-модифицирующие средства (анальгетики и НПВП — нестероидные противовоспалительные препараты), купирующие боль и воспаление в суставах, и симптоматические лекарственные средства замедленного действия [3, 14]. Симптоматические лекарственные средства замедленного действия (SYSADOA — Symptomatic Slow Activity Drugs for Osteoarthritis) [3, 14] — класс разнообразных препаратов, которые положительно влияют на симптомы ОА и имеют доказательства болезнь-модифицирующего действия при их длительном применении. Метаанализы плацебо-контролируемых исследований SYSADOA доказали, что они оказывают не только симптоматическое действие, но и замедляют прогрессирование ОА за счет противовоспалительного, анаболического, антикатаболического и анальгетического действия. В эту группу входят хондроитина сульфат (ХС), глюкозамина сульфат, неомыляемые соединения авокадо и сои, диацереин и гиалуроновая кислота.
Хондроитина сульфат способен связываться с белками-рецепторами на поверхности хондроцитов, синовиоцитов и остеобластов [15], что приводит к ингибированию воспалительных сигнальных путей, запущенных в результате активации рецепторов. Как следствие, в тканях сустава уменьшаются воспаление, деградация хряща, разрушение костной ткани, образование сосудов в зоне воспаления (ангиогенез) и апоптоз клеток [16]. Кроме того, хондроитина сульфат обладает довольно выраженным действием на боль. Недавно опубликованное исследование показало эффективность ХС в отношении уменьшения структурных изменений в суставах с параллельным симптоматическим клинически значимым действием [9, 17]. Хондропротекторы природного происхождения применяются в ревматологии более 25 лет. Эффективность группы была показана в нескольких клинических исследованиях [18–20].
Однако наука не стоит на месте, и разрабатываются новые препараты, отвечающие всем современным требованиям. Одним из инъекционных хондропротекторов последнего поколения является российский препарат АМБЕНЕ® БИО с уникальным составом, который производится по современной технологии биоэкстракции, относится к инъекционным хондропротекторам последнего поколения. Использование этой технологии позволяет:
- получить экстракт с определенным количеством действующего вещества (100 мг экстракта/1 мл), что обеспечивает предсказуемые результаты терапии;
- приготовить раствор высокой чистоты (за счет инновационной системы нанофильтрации), что способствует хорошей переносимости;
- получить низкий молекулярный вес пептидов, входящих в состав
АМБЕНЕ®БИО, что повышает возможности точечной доставки экстракта к пораженным суставам; / получить раствор с определенным рН (5–7), что обеспечивает антигиалуронидазную активность и противовоспалительное действие препарата [21].
Наблюдательная многоцентровая программа «Сравнительное рандомизированное исследование эффективности и безопасности препарата АМБЕНЕ® БИО при первичном и вторичном остеоартрите различной локализации — КОЛИБРИ» показала высокую эффективность препарата в лечении пациентов с ОА различной локализации [21]. Применение АМБЕНЕ® БИО представляет интерес для использования у пациентов с ОА и коморбидностью, а также с целью поиска новых эффективных средств лечения ОА.
Клинический случай
На амбулаторный прием в октябре 2021 года обратилась женщина 65 лет, русская, москвичка. Жалобы на боли в области коленных суставов в течение последних десяти дней, больше справа, возникающие после ночного сна при начале движений («стартовые боли»), при подъеме по ступенькам, при ходьбе более 10 минут. В покое боль уменьшается, во время сна боль не беспокоит. При оценке по визуальной аналоговой шкале (ВАШ) интенсивность боли при движении составила 58, в покое — 30. По шкале WOMAC индекс по подшкале боли составил 25 баллов, скованности — 9, функции — 88, суммарно — 122 балла. Из анамнеза известно, что пациентка страдает остеоартритом коленных суставов в течение последних 5 лет. Отмечает периодические сезонные обострения весной и осенью. При обострениях принимает пероральные НПВП (ибупрофен) с положительным эффектом. Во время последнего обострения отметила появление болей в эпигастрии к концу противовоспалительного лечения (на 6–7 день), вследствие чего самостоятельно отменила прием препарата.
Имеет сопутствующие заболевания: гипертоническая болезнь II ст. (принимает постоянно антигипертензивные препараты), хронический гастрит, ожирение I ст. Рост — 163, вес — 87 кг, ИМТ — 32,7 кг/м2, рабочее АД 1 — 40/85. При осмотре обоих коленных суставов отмечается сглаженность контуров, более выраженная справа, и нарушение оси конечности в виде умеренной вальгусной девиации справа. Походка нарушена, определяется хромота. Ходит без дополнительной опоры, прихрамывая на правую ногу. Определяется сгибательная контрактура, дефицит амплитуды при сгибании 8°. Диапазон разгибания в обоих коленных суставах полностью сохранен.
Пальпаторно определяется умеренно выраженный периартикулярный отек, больше справа. Пальпация в проекции суставных щелей умеренно болезненна, более выражена по медиальной поверхности обоих коленных суставов, интенсивность больше справа. Флотация надколенника не определяется, синовита нет. При обследовании подколенных ямок признаков наличия кист Бейкера на выявлено. Локальная гипертермия области коленных суставов не определяется. Клинических проявлений повреждения мениска, связочного аппарата не обнаружено.
Пациентке проведено лабораторно-инструментальное исследование. Общий анализ крови без отклонений от нормы. Показатели воспалительной активности в биохимическом анализе крови не выходят за пределы референсных значений.
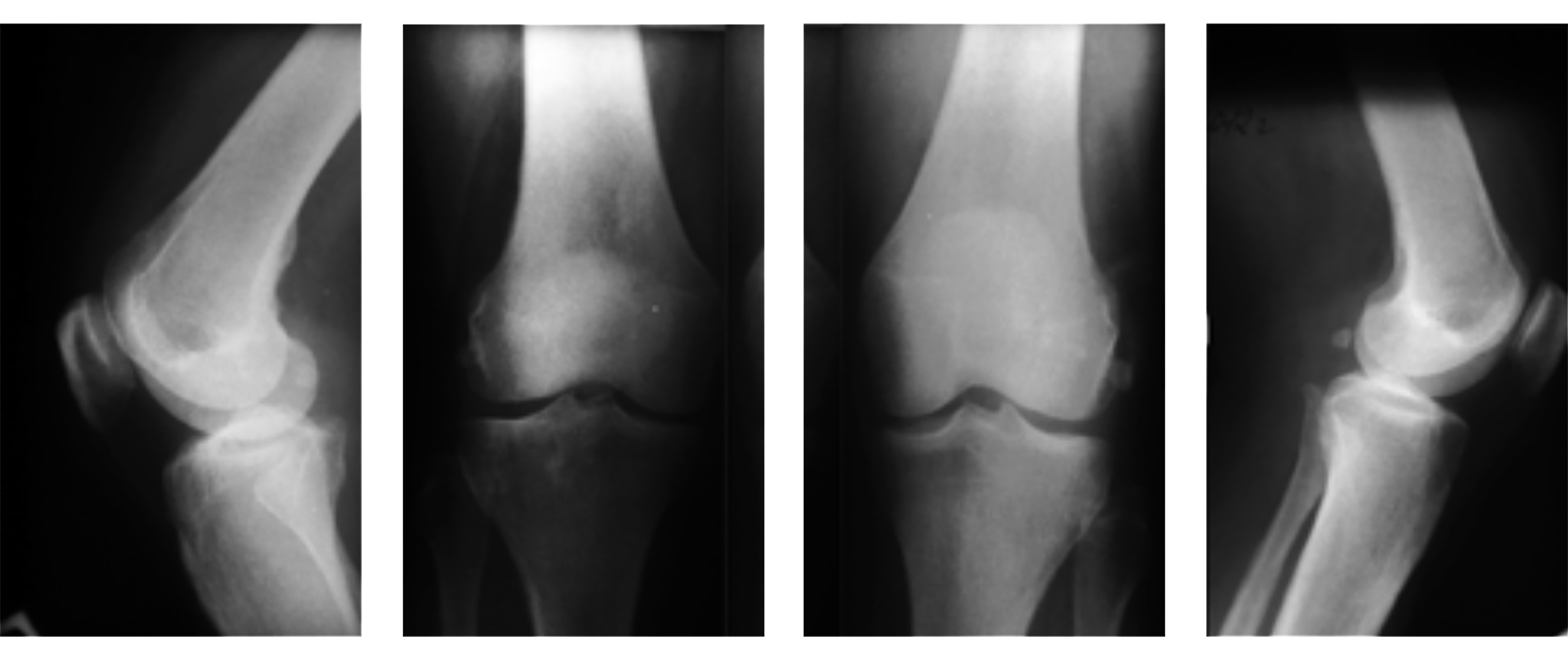
Рис. 1 Рентгенография обоих коленных суставов в прямой и боковой проекциях в положении стоя
Выполнена обзорная рентгенография обоих коленных суставов в двух проекциях в положении стоя (рис. 1). Выявлены признаки субхондрального склероза суставных поверхностей, диффузного остеопороза, заострение межмыщелкового возвышения, умеренно выраженные остеофиты мыщелков большеберцовой и бедренной костей по медиальной поверхности. Учитывая жалобы, данные клинического осмотра и дополнительных методов исследования, пациентке поставлен диагноз: билатеральный остеоартрит коленных суставов II стадии, фаза обострения.
В качестве немедикаментозной терапии больной предложено ношение ортезов с армированными вставками на оба коленных сустава, а также использование индивидуальных ортопедических стелек.
Ввиду наличия у пациентки коморбидности по гастроэнтерологической патологии, гипертонической болезни, а также нежелания принимать пероральные препараты для лечения ОА, нами было решено провести монотерапию препаратом АМБЕНЕ® БИО. Курс состоял из 10 внутримышечных инъекций по 1 мл с интервалом через 1 день. Проводили оценку эффективности лечения через 10 и 20 дней от начала лечения, затем через 2 и 6 месяцев после окончания лечения.
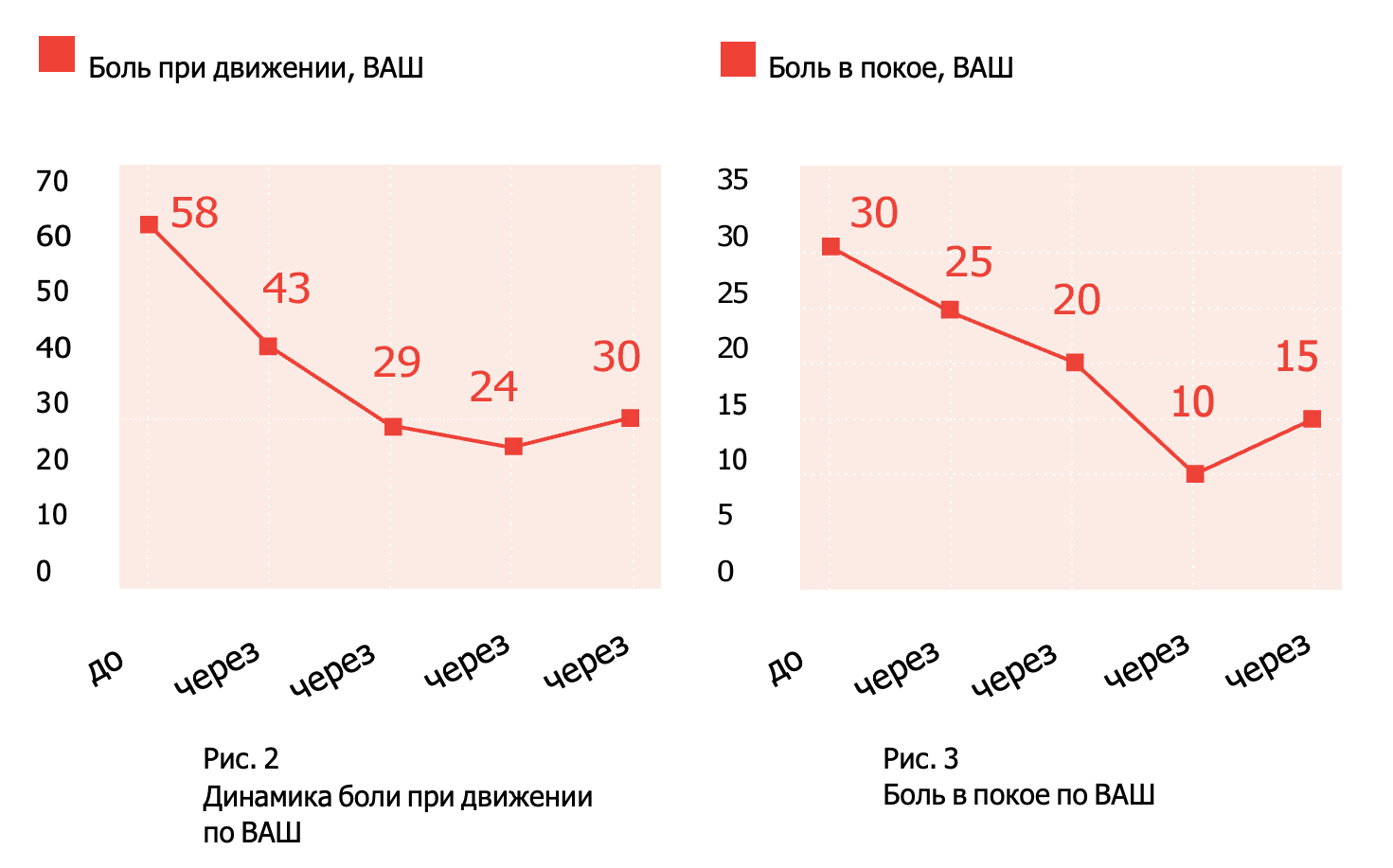
Через 10 дней после начала лечения пациентка отметила уменьшение боли при движении и в покое. Оценка по ВАШ составила 43 и 25, соответственно, т. е. уменьшение боли при движении — на 25,9% и в покое — на 27% (рис. 2, 3). Индекс WOMAC также снизился и составил в подшкале боли — 20 (снижение на 20%) (рис. 4), в подшкале скованности движений — 6 (снижение на 33,3%) (рис. 5), в подшкале функциональности — 70 (снижение на 21,5%) (рис. 6). Суммарный индекс WOMAC снизился на 21,3% и составил 96 (рис. 7).
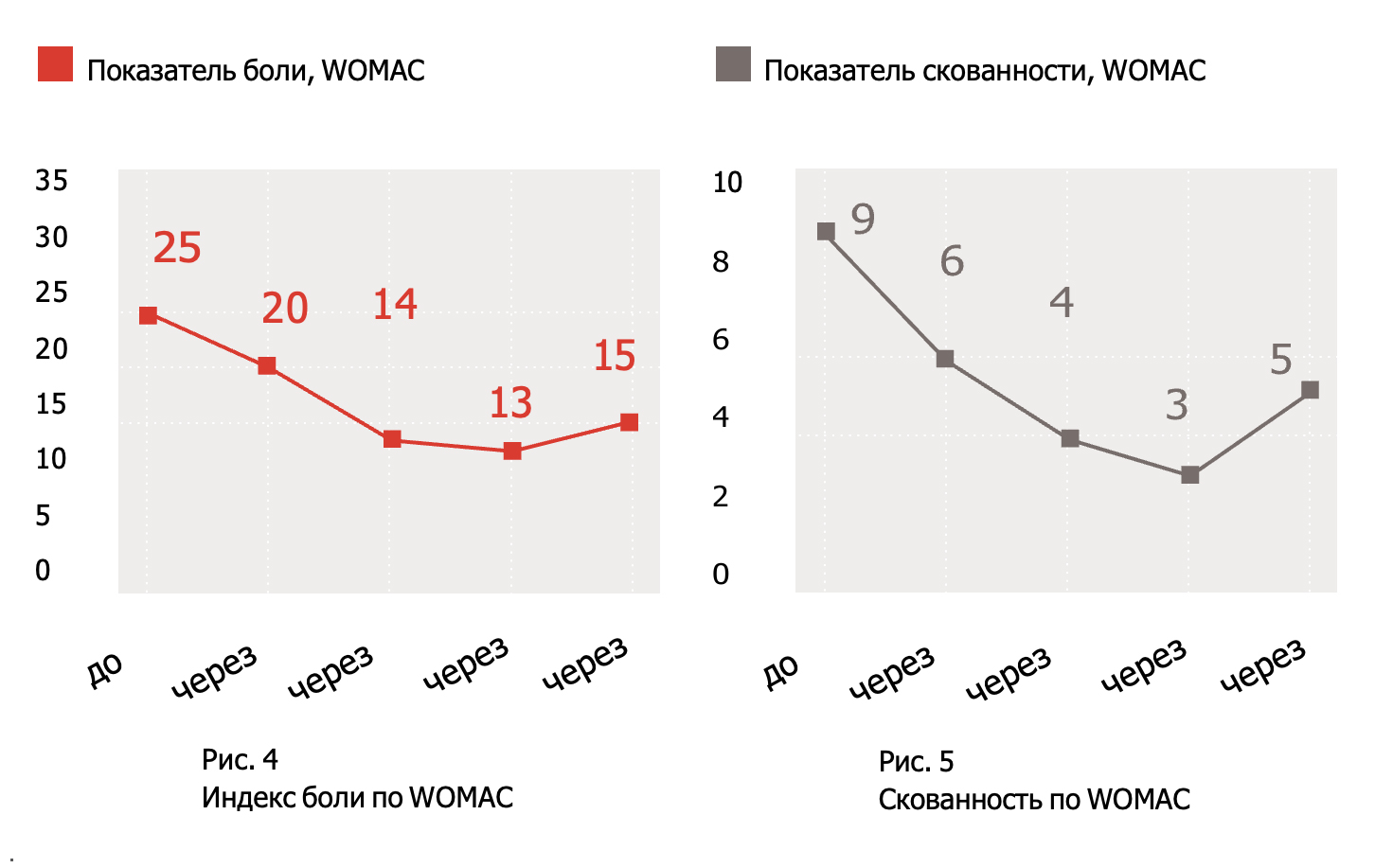
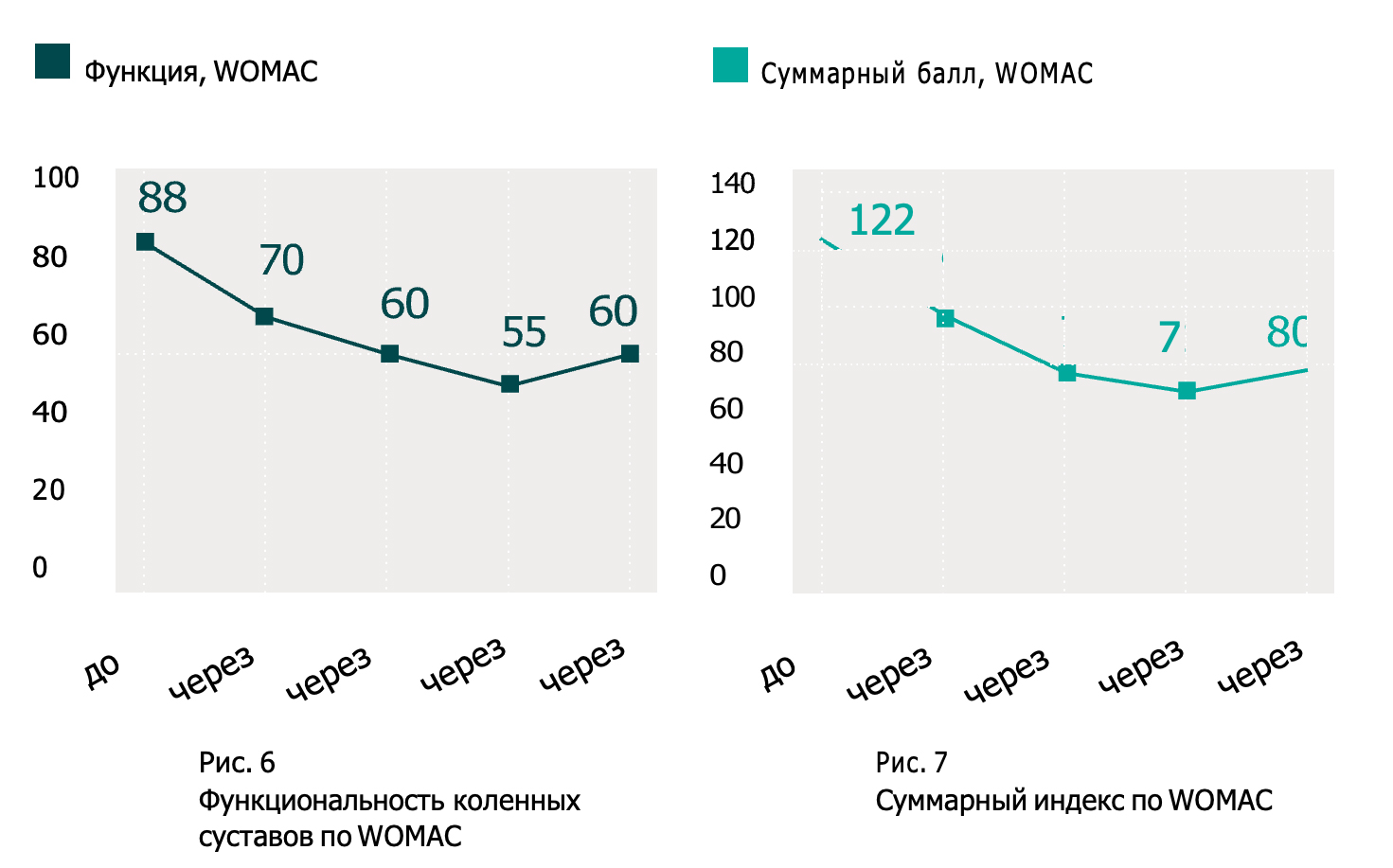
Пациентка продолжила курс лечения АМБЕНЕ® БИО. В течение следующих 10 дней было сделано еще 5 внутримышечных инъекций с интервалом 1 день, после чего проведена очередная оценка эффективности лечения. Отмечено дальнейшее уменьшение болей и улучшение функциональности коленных суставов. Боль при движении по ВАШ снизилась на 50% от исходной и составила 29, в покое — снизилась на 33,3% от исходной и составила 20 баллов. Индекс WOMAC суммарный снизился до 78 (на 36% от исходного показателя), в подшкалах боли — до 14 (на 44% от исходного), скованности — до 4 (на 55,6%), функциональности — до 60 (на 31,8%).
Мы оценили состояние пациентки через 2 месяца после окончания курса лечения. Было отмечено дальнейшее улучшение показателей боли по ВАШ при движении на 58%, в покое — на 66,7%, индекса WOMAC — на 41,8% (подшкала боли — на 48%, скованности — на 33,3%, функции — на 37,5%).
За время наблюдения побочных эффектов и осложнений терапии не выявлено.
Через 6 месяцев наблюдения мы отметили некоторое возрастание симптоматики остеоартрита. Показатели боли по ВАШ составили 30 при движении и 15 в покое, WOMAC — 80 (подшкала боли — 15, скованности — 5, функции — 60). Полагаем, это начало нового сезонного обострения, требующее повторной коррекции. Пациентка изъявила желание повторить курс лечения препаратом АМБЕНЕ® БИО, что может свидетельствовать о высокой приверженности к терапии.
Обсуждение
Терапия остеоартрита коленных суставов имеет несколько целей: / уменьшение воспаления;
- снижение уровня боли;
- улучшение состояния хряща. Выбор терапии ОА затрудняется наличием у пациентов коморбидновости.
Наряду с немедикаментозным лечением в качестве препарато в первой линии рекомендовано использование НПВП и структурно-модифицирующих препаратов (SYSADOA).
В нашем случае пациентка имела коморбидность в виде гипертонической болезни II ст., ожирения I ст., хронического гастрита. В то же время течение ОА не носило агрессивный характер (обострения были сезонными), стадия ОА не была тяжелой или терминальной. Кроме того, предыдущее лечение ОА вызвало обострение хронического гастрита у пациентки, что снизило ее приверженность к терапии ОА в целом. Это позволило нам сделать выбор в пользу терапии с потенциально меньшим количеством побочных эффектов, хотя и с несколько замедленным действием, а именно — препарат из группы структурно-модифицирующих препаратов АМБЕНЕ® БИО.
Современный инъекционный хондропротектор последнего поколения АМБЕНЕ® БИО способствует эффективному снижению боли за счет синергии 4 компонентов. Помимо хондроитина сульфата, в его состав входят 15 аминокислот, пептиды микро и макроэлементы. Благодаря комплексному составу АМБЕНЕ® БИО, хрящевая ткань получает дополнительный субстрат для синтеза новых структурных единиц, что критически важно для увеличения эффективности терапии. Вследствие своего уникального состава и синергичности 4 компонентов, АМБЕНЕ® БИО оказывает патогенетическое влияние на проблемные суставы и не только облегчает боль и восстанавливает нарушенное функционирование, но и способствует снятию воспаления, прекращению деградации хряща и восстановлению хрящевой ткани [21, 22].
У нашей пациентки удалось, не прибегая к использованию НПВП, достичь заметного снижения воспалительной активности и устойчивого снижения интенсивности боли. Это позволяет рассматривать АМБЕНЕ® БИО как препарат выбора базисной терапии у пациентов с начальными стадиями остеоартрита и коморбидностью.
Одно из преимуществ АМБЕНЕ® БИО — современная технология производства — биоэкстракция, благодаря которой препарат обладает высокой эффективностью и благоприятным профилем безопасности. У АМБЕНЕ® БИО зарегистрирована удобная короткая схема применения, позволяющая за непродолжительный курс из 10 инъекций обеспечить длительный эффект до 6 месяцев [23].
В результате проведенного лечения мы получили ожидаемый эффект в виде снижения интенсивности воспалительного процесса и уменьшения боли. Что касается такой цели терапии, как поддержка состояния хряща и предотвращение его деградации, это будет предметом наблюдения при ведении пациентки в дальнейшем. Следует отметить высокую комплаентность больной, удовлетворенность эффективностью лечения и отсутствием побочных эффектов, что выразилось в желании использовать АМБЕНЕ® БИО при возникновении следующего сезонного обострения.
Вывод
У нашей пациентки удалось, не прибегая к использованию НПВП, достичь заметного снижения воспалительной активности и устойчивого снижения интенсивности боли. Это позволяет рассматривать АМБЕНЕ® БИО как препарат выбора базисной терапии у пациентов с начальными стадиями ОА и коморбидностью.
Литература
- Новосёлов К.А., Корнилов Н.Н., Куляба Т.А. Повреждения и заболевания коленного сустава. Глава 5. Травматология и ортопедия / Н.В. Корнилов. — СПб: Гиппократ, 2006; 3:213–438.
- Мартынов А.И., Наумов А.В., Верткин А.Л. и др. Ведение больных с остеоартритом и коморбидностью в общей врачебной практике: мнение экспертов, основанное на доказательной медицине. Лечащий врач. 2015; 04:39–46.
- Гонартроз. Клинические рекомендации РФ 2021. https://cr.minzdrav.gov.ru/ schema/667_1
- Sun X, Zhen X, Hu X, et al. Osteoarthritis in the Middle-Aged and Elderly in China: Prevalence and Influencing Factors. Int J Environ Res Public Health. 2019 Nov 26; 16(23).
- Vina ER, Kwoh CK. Epidemiology of osteoarthritis: literature update. Curr Opin Rheumatol. 2018 Mar; 30(2):160–167.
- Tachmazidou I, Hatzikotoulas K, Southam L, et al. Identification of new therapeutic targets for osteoarthritis through genome-wide analyses of UK Biobank data. Nat. Genet. 2019; 51(2):230– 236.
- Hassanali SH, Oyoo GO. Osteoarthritis: a look at pathophysiology and approach to new treatments: a review. East African Orthopaedic Journal. 2011; 5:51–57.
- Glasson S. Identification of targets through histologic evaluation of osteoarthritis in knockout mice. Osteoarthritis Cartilage. 2005; 13(3).
- Лила А.М., Алексеева Л.И., Таскина Е.А. Современные подходы к терапии остеоартрита с учетом обновленных международных рекомендаций. РМЖ. Медицинское обозрение. 2019; 3(11-II):48– 52.
- Veronese N, Cereda E, Maggi S, et al. Osteoarthritis and mortality: A prospective cohort study and systematic review with meta-analysis. Semin Arthritis Rheum. 2016 Oct; 46(2):160–167. DOI: 10.1016/j.semarthrit.2016.04.002.
- Kovari E, Kaposi A, Bekes G, et al. Comorbidity clusters in generalized osteoarthritis among female patients: A cross-sectional study. Semin Arthritis Rheum. 2019 Sep 9; S0049–0172(19)30233– 1. DOI: 10.1016/j.semarthrit.2019.09.001.
- Bijlsma JW, Berenbaum F, Lafebern FPJ. Osteoarthritis: an update with relevance for clinical practice. Lancet. 2011; 377(9783):2115–2126.
- Bannuru RR, Osani MC, Vaysbrot EE, et al. OARSI guidelines for the nonsurgical management of knee, hip, and polyarticular osteoarthritis. Osteoarthritis Cartilage. 2019 Nov; 27(11):1578–1589. DOI: 10.1016/j.joca.2019.06.011.
- Bruyere O, Honvo G, Veronese N, et al. An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO). Semin Arthritis Rheum. 2019 Apr 30; S0049–0172(19)30043–5. DOI: 10.1016/j.semarthrit.2019.04.008.
- Lo YL, Sung KH, Chiu CC, Wang LF. Chemically conjugating polyethylenimine with chondroitin sulfate to promote CD44mediated endocytosis for gene delivery. Mol Pharm. 2013 Feb 4; 10(2):664–676. DOI: 10.1021/mp300432s. Epub 2013 Jan 14.
- Духанин А.С. Симптоммодифицирующие препараты замедленного действия в лечении остеоартрита: от молекулы к клиническому эффекту (взгляд фармаколога). Современная ревматология. 2018; 12(2):79–87. DOI:
- 14412/1996-7012-2018-2-79-87. 17. Алексеева Л.И., Таскина Е.А., Лила А.М. и др. Многоцентровое проспективное рандомизированное исследование эффективности и безопасности препарата Алфлутоп® в альтернирующем режиме по сравнению со стандартным режимом. Сообщение 1: оценка эффективности препарата при различных схемах применения. Современная ревматология. 2019; 13(3):51–59. DOI: 10.14412/1996-70122019-3-51-59.
- Bartels EM, Bliddal H, Schondorff PK, et al. Symptomatic efficacy and safety of diacerein in the treatment of osteoarthritis: a meta-analysis of randomized placebo-controlled trials. Osteoarthr Cartil. 2010; 18(3):289–296. DOI: 10.1016/j.joca.2009.10.006.
- Towheed TE, Maxwell L, Anastassiades et al. Glucosamine therapy for treating osteoarthritis. Cochrane Database Syst Rev. 009; 2:CD002946. DOI: 10.1002/14651 858.cd002 946.pub2.
- Singh JA, Noorbaloochi S, MacDonald R, Maxwell LJ. Chondroitin for osteoarthritis. Cochrane Database Syst Rev. 2015; 1:CD005614. DOI: 10.1002/14651858. CD005614.
- Меньшикова И.В., Сороцкая В.И. Лечение остеоартроза крупных и мелких суставов с использованием инъекционного хондропротектора комплексного действия. Лечащий врач. 2021; 4(24):66–71. DOI: 10.51793/ OS.2021.14.17.012.
- Данилов А.Б., Зоткин Е.Г. Медицинский дуэт: остеоартрит и остеохондроз — консенсус невролога и ревматолога. Эффективная фармакотерапия. 2022; 3.
- 23. Нормативная документация: Фармакопейная статья на субстанцию жидкость «биоактивный экстракт из мелкой морской рыбы»